Работа со щелочными металлами. Источники опасности
Щелочные металлы широко применяются в лабораториях в качестве реагентов для синтеза и анализа, активных восстановителей, а также осушителей для органических растворителей. Эти металлы относятся к наиболее активным элементам, что обуславливает их высокую пожаровзрывоопасность, а также агрессивность по отношению к тканям организма. Чрезвычайно опасны ожоги расплавленными щелочными металлами. Термические ожоги в этом случае усугубляются тяжелыми химическими ожогами. Любые операции с дисперсиями щелочных металлов, а также с металлическим калием справедливо считаются одними из самых опасных работ в химической лаборатории.
Все эти металлы сходны по своим физико-химическим свойствам. Однако для разработки конкретных мер предосторожности при работе с ними недостаточно знать их общие свойства. Поэтому рассмотрим свойства каждого щелочного металла в отдельности и связанные с этими свойствами источники Опасности [8].
Литий (плотность 0,534 г/см3, температура плавления 180,5 °С). Распространенным заблуждением в лабораторной практике является надооценка опасности, которую представляет металлический литий. Действительно, реакционная способность лития существенно ниже, чем калия и натрия. Однако степень опасности того или иного вещества не всегда находится в прямой зависимости от его химической активности, и в некоторых отношениях литий опаснее натрия. Тушенце горящего лития, например, представляет гораздо более серьезную проблему, чем тушение натрия и даже калия.
При работе с литием следует учитывать, что он обладает наименьшей плотностью из всех твердых и жидких веществ. Литий, в отличие от калия и натрия, всплывает в любом органическом растворителе. Поэтому его нельзя хранить в керосине или жидком масле. Подходящей средой для хранения лития служит вазелин или парафин.
При нормальной температуре литий медленно взаимодействует с кислородом воздуха. При повышении температуры реакция идет более бурно, и при температуре выше точки плавления металл может самовоспламениться. Присутствие оксида или нитрида способствует самовоспламенению.
Иногда взаимодействие тонкой суспензии лития с галогеналкилами и галогенарилами (например, при получении фениллития из бромбензола в эфире) протекает, после некоторого индукционного периода-чрезвычайно бурно. Полагают, что такое течение реакции может быть связано с наличием на частицах металла оксидной пленки, которая исчезает в результате химической реакции или при перемешивании, обнажая сразу большую поверхность металла.
Взаимодействие лития с ртутью для получения амальгамы экзотермично и при использовании большого куска лития может привести к взрыву. Так же опасно сплавление лития с алюминием, висмутом, кальцием, свинцом, оловом и некоторыми другими металлами.
Литий используют для восстановления некоторых металлов из их оксидов. После инициирования при умеренной температуре реакция протекает бурно. Взаимодействие оксида хрома(III) с литием начинается при 180 °С, а в ходе реакции смесь разогревается до 965°С. Ниже приведены начальная и конечная температуры при взаимодействии лития с некоторыми оксидами:
Восстановленный таким способом металл содержит избыток лития, поэтому оставленная на воздухе масса иногда воспламеняется.
Натрий (плотность 0,97 г/см3, температура плавления 97,7 °С). Вследствие высокой химической активности натрия работа с ним в лаборатории представляет серьезную опасность. В то же время натрий широко применяется для абсолютирования углеводородов и простых эфиров. Частая работа с ним приводит к известному психологическому эффекту — адаптации к опасности [29]. Даже опытные работники иногда грубо нарушают правила обращения с металлическим натрием. Ежегодно по этой причине в химических лабораториях происходит значительное число взрывов и пожаров.
Натрий взаимодействует с кислородом воздуха при комнатной температуре с образованием оксида. Реагируя с влагой воздуха, оксид переходит в гидроксид. Куски натрия, оставленные на воздухе, быстро обрастают расплывающейся коркой гидрокси-да. Такие куски ошибочно могут быть приняты за один из обычно применяемых осушителей. При мытье посуды водой в таких случаях иногда происходят взрывы, которые особенно опасны из-за их неожиданности. К тому же лаборанты при мытье посуды нередко работают без очков. Во избежание несчастных случаев следует уничтожать остатки натрия сразу после их образования. Во влажном воздухе достаточно большие куски через некоторое время могут воспламениться. Дисперсии металлического натрия в угле„-водородах немедленно воспламеняются на воздухе при удалении растворителя.
Сотрудник А. выполнял работу, связанную с получением и использованием дисперсии металлического натрия в органическом растворителе. До атого ему неоднократно приходилось работать со щелочными металлами, однако с необходимостью получения дисперсии он столкнулся впервые. В оригинальной статье, откуда сотрудник заимствовал методику работы, ничего не говорилось о повышенной опасности дисперсий щелочных металлов, указывалось только, что все манипуляции необходимо проводить в аргоне.
Сотрудник приготовил дисперсию натрия в толуоле в колбочке вместимостью 200 мл под аргоновой «подушкой», затем вылил в токе аргона полученную дисперсию в литровую реакционную колбу и отложил пустую колбочку на поддон для грязной посуды, стоящий рядом с установкой в вытяжном шкафу. Он заметил, что на стенках и горле колбочки остался налет мелкораздробленного натрия, и собирался ополоснуть ее спиртом. Однако сразу же, как только в колбочку попал воздух, произошла вспышка. Сотрудник инстинктивно отдернул руки и при этом уронил капельную воронку, содержащую 200 мл органического растворителя. Воронка разбилась, растворитель воспламенился, огонь охватил реакционную колбу. К счастью колба не разбилась и пожар удалось сравнительно быстро ликвидировать с помощью углекислотных огнетушителей.
При анализе происшествия выяснилось, что сотрудник не знал о том, что дисперсии натрия мгновенно воспламеняются в воздухе. За три месяца до этого он сдал экзамен по технике безопасности, однако в инструкции по работе со щелочными металлами не были упомянуты свойства дисперсии. Во время предварительного обсуждения работы с руководителем сотрудник не информировал его о том, что собирается заменить обычно используемую натриевую проволоку дисперсией, считая это несущественной деталью.
Теплоты реакции часто бывает достаточно для воспламенения образующегося водорода. При растворении небольших кусочков натрия в холодной воде (ниже 40 °С) воспламенения, как правило, не происходит. Однако, если подвижность кусочков натрия ограничена (например, они помещены в вязкий раствор или на мокрую фильтровальную бумагу), воспламенение неизбежно. Особенно опасен контакт натрия с водой в условиях, когда выделяющийся водород накапливается в ограниченном объеме, например при попадании воды в колбу с остатками натрия; следствием обычно бывает взрыв воздушно-водородной смеси. При контакте натрия со льдом происходит взрыв.
Присутствие воды в спирте значительно ускоряет реакцию. Взаимодействие этилового спирта, содержащего более 5% воды, с натрием небезопасно. При реакции натрия со спиртами следует также принимать меры против образования взрывоопасной воздушно-водородной смеси.
Студент-дипломник Л. собирался уничтожить остатки натриевой проволоки в бутылке из-под растворителя. Держа бутылку в руках, он налил в нее небольшое количество этилового спирта. Реакция оказалась чрезвычайно бурной, натрий сразу же расплавился, бутылка сильно разогрелась. Л. поставил бутылку в раковину и отскочил в сторону. От соприкосновения с холодной водой бутылка треснула, несколько шариков расплавленного натрия попало в раковину и затем через сливную решетку — в канализационную трубу. Через несколько секунд последовал взрыв, разрушивший чугунный сифон. Никто из присутствующих'не пострадал.
При расследовании происшествия выяснилось, что работавшие в лаборатории студенты и сотрудники регулярно снимали УФ-спектры в 96% этиловом спирте. Отходы спирта сливались в емкость с надписью «Сливы этанола (после УФ-спектров)» и обычно использовались для технических целей, главным образом, для уничтожения отходов натрия. За день до происшествия, с разрешения преподавателя, в комнате работала студентка из другой лаборатории —снимала УФ-спектры в водно-спиртовом растворе. После окончания работы она без ведома сотрудников вылила остатки растворов в емкость для сливов. Анализ солепжимого бутылки ппкячял что Л., не зная того, использовал для уничтожения натрия фактически 50% водно-спнртовый раствор.
Примечательно, что лицами, имеющими отношениенк аварии, фактически не было допущено какого-либо серьезного нарушения правил. Однако все они в той или иной степени проявили недостаточную осмотрительность. В результате произошла авария, последствия которой могли быть гораздо более серьезными.
С горячим глицерин-ом натрий реагирует бурно, выделяющийся водород немедленно воспламеняется, поэтому использование глицериновых бань для нагревания установок, содержащих натрий, не менее опасно, чем использование водяных бань.
С диоксидом углерода, в отличие от лития, натрий не реагирует вплоть до температуры красного каления. Однако- загоревшийся натрий продолжает гореть после вытеснения воздуха диоксидом углерода, причем интенсивность горения увеличивается. Контакт твердого диоксида углерода (сухого льда) с. натрием приводит к сильному взрыву.
В отличие от лития, натрий не реагирует с азотом, горение металла в атмосфере азота прекращается.
Смеси натрия с галогенпроизводными углеводородов, за исключением полностью фторированных, взрываются от удара или сжатия, а также при повышении температуры. Мелкораздробленный натрий взаимодействует с неразбавленными галоген-алкилами и галогенарилами со взрывом. Критическим фактором при взаимодействии натрия с галоген-производными углеводородов служит температура. Так, при получении бутилбензола по реакции Вюрца из бромбензола и 1-бромбутана в присутствии натрия в среде эфира при температуре ниже 15 °С реакция почти не идет. Выше 15 °С реакция идет достаточно активно, а выше 30 °С выходит из-под контроля [64].
В литературе имеются сообщения и о непредсказуемом течении реакций. Так, небольшая проба (около 1 г) перфторгексилиодида не реагировал при кипении (114 °С) с натрием, а смесь 140 г указанного иодида и 7 г натрия взорвалась через 30 мин [59]. Следует соблюдать осторожность в ходе сплавления органических соединений с натрием при выполнении качественного анализа. Наличие галогенпроизводных в пробе
Получение амальгамы натрия путем прямого контакта с ртутью сопровождается значительным выделением теплоты. При отсутствии. мер предосторожности температура может достичь 400 °С. Во избежание взрывов и разбрызгивания ртути взаимодействие следует либо проводить под слоем инертной защитной жидкости, например толуола или минерального масла, либо постепенно добавлять ртуть к натрию из капельной воронки.
Дисперсии натрия в эфире, толуоле или тетрагидро-фуране применяются для восстановления многих металлов из их галогенидов. Получаемые таким способом порошки кадмия, хрома, кобальта, меди, железа, марганца, молибдена, никеля, алюминия, олова, цинка, индиЯ, магния и других металлов обладают высокой химической активностью и пирофорны. Смеси натрия с галогенидами металлов чувствительны к удару. При этом хлорид и бромид железа(III), бромид и иодид железа(II), хлорид и бромид кобальта(II) вызывают очень сильные взрывы. Сильные взрывы дают смеси натрия с галогенидами алюминия, сурьмы, мышьяка, висмута, меди(II), ртути, серебра, свинца, а также с пентахлоридом ванадия. Хлорид алюминия, галогениды меди(1), кадмия, никеля дают слабые взрывы. Смеси натрия с галогенидами щелочных и щелочноземельных металлов невзрывоопасны.
Чувствительны к удару смеси натрия с органическими соединениями, содержащими нитрогруппы, например с нитрометаном, нитробензолом, динитробензолом, динитронафталином, этил-нитритом, этилнитратом, тринитроглицерином и др. Взрывоопасное™ смесей повышается с увеличением числа нитрогрупп.
Безводные хлороводород, фтороводород и серная кислота медленно реагируют с натрием. Контакт водных растворов кислот с металлом вызывает взрыв.
Калий (плотность 0,87 г/см3, температура плавления 63,7 °С). По химическим свойствам калий сходен с натрием, а по активности превосходит его. Во всех отношениях калий представляет гораздо более серьезную опасность, чем натрий.
Во влажном воздухе окисление идет настолько быстро, что металл расплавляется и может воспламениться, особенно при локальном применении давления и обнажении свежей поверхности, например при выдавливании проволоки.
При длительном контакте с воздухом куски калия покрываются плотной коркой надпероксида калия с промежуточной прослойкой из оксида.
Взаимодействие надпероксида калия со способными окисляться органическими или неорганическими веществами настолько активно, что может сопровождаться взрывом. Взрыв возможен уже при простом соприкосновении органическиx веществ с сильно окислившимися кусками калия.
При срезании корки оксидов с кусков калия нередко происходит воспламенение или даже взрыв. Хотя контакт свежеочищенной поверхности' калия с чистым надпероксидом калия приводит только к воспламенению после некоторого индукционного периода, присутствие следов воды, примесей углеводородных растворителей или минерального масла значительно увеличивает вероятность взрыва.
Старые, сильно окислившиеся куски калия, у которых корка оксидов окрашена в желтый или желто-оранжевый цвет, использовать нельзя. Они должны быть уничтожены добавлением небольших порций грег-бутилового спирта в фарфоровом стакане под слоем ксилола.
Взаимодействие калия даже с холодной водой протекает настолько бурно, что выделяющийся водород немедленно воспламеняется. При контакте крупных кусков калия с водой происходит взрыв, мелкие брызги горящего расплавленного металла разлетаются (иногда в радиусе нескольких метров), вызывая вторичные очаги загорания, а при попадании на кожу — очень опасные ожоги: Взрываются и мелкие кусочки калия в случае их контакта с ограниченным количеством воды, например при попадании на влажные поверхности.
Со спиртами калий реагирует гораздо энергичнее, чем натрий. Попытки получения алкоголятов путем добавления калия к спиртам (включая октанол, бен-зиловый спирт, циклогексанол) приводят к взрыву, если воздух из реакционного сосуда не был предварительно вытеснен азотом или аргоном. Вносить калий в спирты рекомендуется очень небольшими порциями при перемешивании, обязательно контролируя температуру массы. Добавлять очередную порцию калия следует только после охлаждения раствора. Необходимо полностью исключить возможность попадания кусочков калия в охлаждающую баню: при контакте калия со снегом или льдом происходит .взрыв.
Сдиоксндом углерода калий реагирует аналогично натрию. С оксидом углерода СО, в отличие от натрия, калий легко реагирует с образованием взрывоопасного карбонила. Реакция идет уже при — 50 °С, продуктом ее является дикарбоннл калия КС2О2. При контакте с воздухом или водой, а также при нагревании до 100 °С последний взрывается. Калий легко реагирует с различными, формами углерода — сажей, графитовым порошком, активным углем. При повышенных температурах реакция протекает весьма бурно. Если углерод находится в мелкодисперсном состоянии, взаимодействие его с калием в присутствии воздуха может происходить со взрывом. Главную роль при этом играет, очевидно, реакция образующегося надпербксида калия с углеродом. Взрывы могут происходить также при попытках погасить горящий калий графитовым порошком, который нередко рекомендуют в качестве огнегасительного средства, что неправильно.
С галогенпроизво'дными углеводородов калий образует взрывоопасные смеси, которые еще более чувствительны к удару и нагреванию, чем смеси с натрием. Взрывоопасность повышается с увеличением числа атомов галогена в молекуле. Так, смесь калия с четыреххлористым углеродом в 150— 200 раз чувствительнее к удару по сравнению с гремучей ртутью, а смесь калия с бромоформом взрывается от ничтожного сотрясения. Смеси с тетра- и пентахлорэтаном склонны взрываться самопроизвольно. Взаимодействие калия с галогенпроизводными углеводородов в инертных растворителях поддается контролю при точном соблюдении условий реакции, в частности температурного режима, однако следует строго следить за тем, чтобы поверхность металла была свежеочищенной — наличие даже следов оксидов приводит к непредсказуемому течению реакции.
С галогенидами. многих металлов калий реагирует аналогично натрию, но более энергично.
Многие органические и неорганические соединения, содержащие н итро груп п у,'например нитрат аммония, пикриновая кислота, нитробензол, будучи нечувствительны к удару сами по себе, становятся чрезвычайно взрывоопасными в присутствии даже следов калия или калий-натриевого сплава.
Сплав калий-натрий. Сплав содержит 50—85% (по массе) калия, температура его плавления ниже комнатной. Химическая активность сплава аналогична активности калия, однако в обращении он еще опаснее. Будучи жидким при комнатной температуре, сплав вступает с реагентами в более тесный контакт, чем твердый металл, поэтому реакции идут еще энергичнее. При контакте с воздухом сплав немедленно воспламеняется, так как легко вытекает из оксидной пленки, обнажая свежую поверхность металла. Смесь сплава с твердым д и о кс и до м углерода в 40 раз более чувствительна к удару по сравнению с гремучей ртутью. Не рекомендуется использовать сплав для восстановления металлов из галогенидов в тех случаях, когда соль хорошо растворима в используемом растворителе (например, ZnCh или FeCl3 в тетра-гидрофуране), поскольку реакция может быть слишком бурной.
Отходы лития. Обрезки и небольшие (не более горошины) кусочки лития можно уничтожить путем растворения в большом количестве холодной воды в вытяжном шкафу.
Дисперсии лития ввиду их высокой реакционной, способности нельзя растворять в воде. Остатки дисперсии в углеводородном растворителе уничтожают постепенным добавлением этилового спирта.
Отходы натрия. Обрезки и остатки проволоки в количествах не более 5—10 г немедленно уничтожают, заливая их в фарфоровом стакане небольшими порциями этилового спирта до полного растворения. Допускается использование изопропилового спирта, содержащего до 2% воды для ускорения реакции. Существует способ уничтожения небольших кусочков натрия в колбе с холодной водой. Поверх воды наливают слой бензина толщиной 3—5 см. Кусочки натрия по одному опускают в колбу. Очередной кусочек вносят только после полного растворения предыдущего. Натрий растворяется на границе раздела фаз, защитный слой бензина препятствует воспламенению водорода. Способ удобен, однако с точки зрения безопасности не имеет преимуществ перед общепринятыми методами.
Необходимо следить за полнотой растворения натрия при обработке этиловым спиртом шламов после проведения реакций: Так, избыток натрия после реакции Вюрца не всегда удается полностью уничтожить спиртом, поскольку кусочки натрия бывают покрыты коркой галогенидов, нерастворимых в спирте. Последующее промывание водой в таких случаях приводит к воспламенению массы.
Дисперсии натрия разлагают добавлением по каплям безводного спирта без доступа воздуха.
Отходы калия. Эти отходы уничтожают, заливая их смесью равных количеств петролейного эфира и безводного изопропилового спирта. Уничтожение остатков калия с помощью этилового спирта является нарушением правил техники безопасности. Обрезки калия можно разлагать в фарфоровом стакане в вытяжпеткой с такой скоростью, чтобы реакция была не слишком бурной. Б случае воспламенения стакан накрывают заранее приготовленным куском асбеста.
Не допускается сбор обрезков калия и натрия в одну емкость. При контакте двух металлов образуется сплав, который при определенном соотношении компонентов становится жидким при комнатной температуре, что значительно повышает опасность работы с ним. Особенно опасно уничтожать сильно окислившиеся куски калия в случае,. если корка оксидов имеет желтую' окраску. Даже с грет-бутиловым спиртом реакция может протекать слишком бурно. Уничтожение проводят в фарфоровом стакане под слоем ксилола, добавляя по каплям грег-бутиловый спирт. Операцию осуществляют в свободном вытяжном шкафу при закрытых створках, имея наготове средства пожаротушения.
Большие количества щелочных металлов. Уничтожение больших количеств иногда рекомендуется проводить путем сжигания на открытых площадках. Однако такие рекомендации нельзя признать обоснованными. При горении щелочных металлов на воздухе образуются аэрозоли гидроксидов в виде дыма, что приводит к загрязнению окружающей среды. Сжигать щелочные металлы можно только в специальных печах, оборудованных системами подачи воздуха и очистки отходящих газов.
При правильной организации работы в лаборатории, когда обрезки не накапливаются, а уничтожаются своевременно, не возникает необходимости уничтожения больших количеств щелочных металлов.
Очистка щелочных металлов от оксидных пленок
Оксидные пленки с поверхности кусков лития и натрия рекомендуется удалять острым ножом под слоем ксилола или минерального масла, предварительно высушенных над натриевой проволокой. Операцию удобно проводить в фарфоровой ступке. Очищенные куски металла переносят пинцетом в счакан или колбочку с высушенным ксилолом. Обрезки металла после осторожного декантирования ксилола немедленно уничтожают. Пои очистке калия эта методика не может считаться безопасной, хотя и рекомендуется в некоторых руководствах. При контакте свежей поверхности калия с оксидной пленкой иногда происходят взрывы даже под слоем защитной жидкости.
Гораздо безопаснее, экономичнее и проще способ очистки калия, заключающийся в плавлении металла под слоем высушенного гептана. Небольшие неочищенные куски (около 20 г) плавят в широкогорлой колбе Эрленмейера или в высоком стакане. После расплавления металла нагревание прекращают и аккуратным вращением колбы добиваются того, чтобы калий вытек из оксидных пленок. Если необходимы более мелкие куски, осторожным встряхиванием колбы или стеклянной палочкой разбивают порцию на несколько глобул. Далее колбу охлаждают и когда металл затвердевает, вынимают глобулы с помощью острой железной палочки или длинного пинцета и переносят в тарированный бюкс с гептаном лля последующего взвешивания. Оставшиеся пленки подлежат немедленному уничтожению:
Описанная методика пригодна и для очистки натрия. В этом случае вместо гептана используют высушенный ксилол.
Нельзя резать щелочные металлы на воздухе, даже если не требуется сохранение блестящей поверхности — это опасно.
Абсолютироваиие органических растворителей
Большая часть аварий и несчастных случаев, связанных с металлическим натрием, происходит при его использовании в качестве осушителя.
Абсолютирование натрием проводится настолько часто, что даже опытные работники иногда забывают об осторожности. Кроме того, эту операцию нередко поручают лаборантам, не проводя подробного инструктажа.
Натрий можно применять для абсолютирования только углеводородов и простых эфиров. Как правило, нельзя использовать натрий для сушки кислот, сложных эфиров, спиртов, галогенпроизводных жирного и ароматического рядов, альдегидов, кетонов, аминов и др.
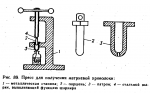
Для получения натриевой проволоки пользуются специальным прессом, изображенным на рис. 89. В патрон помещают небольшие куски натрия, предварительно очищенные от гидроксидной корки. Патрон вставляют в гнездо пресса, к отверстию патрона вплотную приставляют бутылку с растворителем, и затем, медленно вращая винт, выдавливают проволоку. После выдавливания всего натрия поршень вынимают из патрона, помещают их в фарфоровый стакан и заливают этиловым спиртом, чтобы растворить остатки натрия. По окончании растворения поршень и патрон тщательно моют водой и сушат в шкафу.
Если растворитель предполагается оставить над натриевой проволокой на ночь, не следует закрывать сосуд притертой пробкой: выделяющийся водород может создать значительное давление в емкости. В таких случаях необходимо использовать пробку, снабженную хлоркальциевой трубкой.
Для ускорения процесса сушки и более полного удаления воды растворитель кипятят около часа в колбе с обратным холодильником над натриевой проволокой, после чего перегоняют его в сухой приемник, защищенный хлоркальциевой трубкой. Не следует забывать, что для нагревания колбы в таком случае нельзя использовать водяную или глицериновую баню. В качестве Жидкого теплоносителя для бани рекомендуется минеральное масло. Натриевую проволоку, оставшуюся после перегонки, уничтожают в той же колбе сразу после ее охлаждения, заливая достаточным количеством этилового спирта. Оставшееся' в колбе небольшое количество растворителя перед уничтожением остатков проволоки можно не удалять.
Если необходимо получить очень сухой растворитель для особо точных работ, в перегнанный над натрием растворитель добавляют новую порцию проволоки, над которой его и хранят. Критерием качества осушки служит поверхность проволоки — в сухом растворителе она долгое время остается блестящей. Склянку с сухим растворителем над натриевой проволокой помещают в металлический контейнер, дно и стенки которого необходимо выложить асбестовым картоном. Хранят контейнеры в отдельном ящике для ЛВЖ.
Абсолютирование сплавом калий-натрий, жидким при комнатной температуре, дёет значительные преимущества: при легком встряхивании сплав вытекает из оксидной пленки и обнажает свежую поверхность, удаления воды из растворителя, при более энергичном встряхивании сплав распадается на мелкие шарики — в этом случае процесс сушки значительно ускоряется. Однако риск, сопряженный с использованием сплава в качестве осушителя, вряд ли компенсируется этими преимуществами. Сплав , так же как и калий, при контакте с воздухом образует чрезвычайно взрывоопасный перокснд, что представляет-особую опасность при абсолютнровании склонных к образованию пер-оксидов простых эфиров.
При выборе способа пожаротушения следует различать горение собственно щелочных металлов, горение водорода, выделяющегося в процессе взаимодействия металла с водой, и горение органического растворителя в присутствии щелочного металла. Наиболее опасно, когда загорается сам щелочной металл, хотя такие случаи происходят редко.
Тушение лития. Серьезную опасность представляет загоревшийся металлический литий. Использование обычных средств пожаротушения (вода, пена, диоксид углерода, галогенпроизводные углеводородов) либо усиливает горение, либо ведет к взрыву. При темпера-' туре выше 250 °С литий быстро разрушает стекло, кварц, бетона огнеупоры, реагирует с песком. Лнтин продолжает гореть в атмосфере азота и диоксида углерода. Непригодны для тушения хлорид и карбонат натрия, поскольку при контакте с этими солями горящий литий вытесняет натрий. Нельзя применять также порошковые огнетушители, снабженные составами ПС-( н ПС-2, хотя во многих инструкциях их ошибочно рекомендуют для тушения всех щелочных металлов.
Для тушения горящего лития разработаны с п е-циальные порошковые составы ПС-И, ПС-12 и ПС-13 на основе различных флюсов и графита с гидрофобизирующими добавками (см. разд. 3.1). Следует использовать также порошкообразный графит, х л о р и д литий, хлорид калия. При работе с литием помимо обычных средств пожаротушения необходимо иметь наготове достаточное количество одного из перечисленных порошков.
Литий можно потушить также, вытеснив воздух из очага горения аргоном. Подавать аргон следует так, чтобы струя газа не разбрызгивала жидкий металл. После прекращения горения остатки металла следует остудить в токе аргона.
Тушение натрия, калия к сплава и атрий-калий. Наилучшие результаты при тушении этих металлов достигаются путем использования огнетушителей, снаряженных порошками ПС-1 и ПС-2 (см. разд. 3.1). Порошок должен полностью покрыть поверхность горящего металла. Горение прекращается также при засыпании металлов мелким сухим кварцевым песком, кальцинированной содой, мелкой поваренной солью. Поваренная соль предпочтительнее песка, поскольку при высокой температуре натрий и калий могут реагировать с диоксидом кремния.
Рекомендуемый иногда в качестве огнегасительного средства порошкообразный графит пригоден для тушения горящего натрия, но не калия. При горении калия и сплава калий-натрий образуется над-пероксид калия, реагирующий с графитом со взрывом. Непригодны для подавления горения натрия и калия порошковые огнетушители, заряженные составом ПСБ на основе бикарбоната натрия и составом СИ-2, содержа щи м тетр а фторди бро мэта н.
Натрий и калий можно тушить аргоном и азотом. Аргон эффективнее, поскольку существенно тяжелее воздуха.
Диоксид углерода непригоден для тушения натрия и калия, однако углекислотным огнетушителем можно успешно потушить горящий растворитель в присутствии натрия. Обычно натрий не воспламеняется, пока не выгорит весь растворитель, так как пары растворителя защищают металл от контакта с кислородом воздуха. Иногда этот эффект удается использовать при тушении горящего металла. Если на горящий в какой-либо емкости натрий вылить небольшое количество керосина, Образовавшийся в результате очаг пламени можно полностью загасить с помощью углекислотного огнетушителя.
Щелочной металл считается потушенным только после полного остывания. Несгоревшие остатки металла тщательно собирают в толстостенный фарфоровый стакан и уничтожают обычным способом.